Populární témata
#
Bonk Eco continues to show strength amid $USELESS rally
#
Pump.fun to raise $1B token sale, traders speculating on airdrop
#
Boop.Fun leading the way with a new launchpad on Solana.

DailyHealthcareAI
Sdílení výzkumných prací a novinek o aplikacích umělé inteligence v radiologii, patologii, genetice, designu proteinů a mnoha dalších. Pojďme se společně učit!
🚀David Baker preprint z roku @UWproteindesign 👇👇
Co dělá řezání proteinových vazeb tak náročným, že příroda vyvinula specializované enzymy s kovovými kofaktory, aby toho dosáhla?@biorxivpreprint @ETH_en
"Výpočetní návrh cysteinových proteáz"
• Amidové vazby v proteinech mají poločas rozpadu stovek let za fyziologických podmínek, což je činí mnohem stabilnějšími než esterové vazby (přičemž aminové skupiny opouštějí pKa >35 oproti <8 u aktivovaných esterů) a předchozí výpočetní enzymy uspěly pouze s aktivovanými substráty malých molekul esterů, nikoli s energeticky náročným štěpením peptidových vazeb potřebným pro proteázy.
• Výzkumníci použili RoseTTAFold Diffusion 2 pro molekulární rozhraní (RFD2-MI) k návrhu zinkových proteáz z minimálních katalytických motivů, přičemž vytvořili ideální aktivní místo s pěti funkčními skupinami (tři zbytky vazby zinku H1, H2, E1, jednou katalytickou bází E2 a jednou tyrosin stabilizující oxyanionem) založenými na strukturách aminopeptidázy N a astacinu, přičemž provedli oboustranný návrh sekvencí proteázy i substrátu pro zajištění přesného umístění cílové amidové vazby.
• Ze 135 testovaných návrhů v jednom kole 36 % vykazovalo aktivitu (14,7 % u modelů obsahujících pouze zinek a 87,5 % u modelů se zinkovou vodou), přičemž všechny aktivní konstrukce štěpily přesně na zamýšlených místech potvrzených hmotnostní spektrometrií; nejaktivnější konstrukce (substrát Zn45 štěpící ZnO36) dosáhla kcat 0,025 ± 0,002 s⁻¹, KM 26 ± 5 μM a kcat/KM 900 ± 200 M⁻¹s⁻¹, což představuje >10⁸násobné zrychlení oproti nekatalyzované hydrolýze; konstrukce vykazovaly vazbu zinku s Kd mezi 10⁻¹⁰ a 10⁻⁸ M, prokázaly substrátovou specificitu ve 4 z 5 lešení a mohly být přeprogramovány tak, aby štěpily lidský protein TDP-43 relevantní pro onemocnění, přičemž 4 varianty dosáhly ≥80% štěpení po 5 hodinách.
Autoři: Hojae Choi a al Donald Hilvert, Samuel J. Pellock, David Baker
Propojit:

21,12K
Může jazykový model naučit se strukturu RNA bez explicitních strukturálních tréninkových dat?@NatureComms @Tsinghua_Uni
"ERNIE-RNA: jazykový model RNA s reprezentacemi vylepšenými strukturou"
• Stávající RNA jazykové modely přehlížejí strukturální informace v sekvencích, což vede k neúplné extrakci rysů a suboptimálnímu výkonu, navzdory hierarchické organizaci RNA, kde primární sekvence přecházejí do specifických strukturálních konformací, které určují biologické funkce. Tradiční výpočetní přístupy k predikci struktury RNA čelí specifickým výzvám: metody založené na termodynamice jsou omezeny přesností parametrů, metody založené na zarovnání mají potíže bez dostatečných homologních sekvencí a modely hlubokého učení vykazují omezenou generalizaci na neviditelné rodiny RNA. Ačkoliv se objevily RNA jazykové modely ve stylu BERT jako RNA-FM (trénovaná na 23 milionech sekvencí), UNI-RNA (1 miliarda sekvencí, 400M parametrů) a RiNALMo (36M sekvencí, 650M parametrů), nedokážou dostatečně zahrnout strukturální informace, přičemž některé, jako UTR-LM, se snaží tento problém řešit začleněním předpovězených struktur z RNAfold, ale čelí omezením kvůli chybám v predikci a snížené schopnosti generalizace.
• ERNIE-RNA je předtrénovaný jazykový model RNA s 86 miliony parametrů založený na modifikované architektuře BERT s 12 transformátorovými bloky a 12 hlavami pozornosti, trénovaný na 20,4 milionu nekódujících RNA sekvencí z RNAcentral po filtraci sekvencí delších než 1022 nukleotidů a aplikaci odstranění redundance CD-HIT při 100% podobnosti. Model zahrnuje mechanismus pozornosti informovaný o párování bází, který přiřazuje hodnoty 2 pro páry AU, 3 pro páry CG a laditelný parametrový α (původně 0,8) pro páry GU v matici poloh vše proti všemu, čímž nahrazuje člen předpojatosti v první vrstvě transformátoru. Předtrénování používalo modelování maskovaného jazyka s 15 % tokenů náhodně nahrazených, trénováno 20 dní na 24 GPU 32G-V100 pomocí fairseq s základní rychlostí učení 0,0001, 20 000 zahřívacími kroky a 0,01 váhovým poklesem, generující jak mapy pozornosti (L×L×156) a tokenové embeddingy (12×768×L) jako výstupy.
• Pozorovací mapy ERNIE-RNA prokázaly schopnost predikce sekundární struktury RNA s nulovým skóre F1 0,552 na testovací sadě bpRNA-1m, překonávající RNAfold (0,492), RNAstrukturu (0,491), RNAErnie (0,440) a RNA-BERT (0,365) bez jemného ladění. Po doladěním ERNIE-RNA dosáhla špičkových makroprůměrných F1 skóre 0,873 na bpRNA-1m, čímž překonala RiNALMo (0,850, 650M parametrů) a UNI-RNA (0,821, 400 m parametrů), s podobným vedením na ArchiveII (0,954 vs. RiNALMo 0,892) a RIVAS TestSetB (0,721 vs. 0,555 RiNALMo). V náročných testech generalizace napříč rodinami dosáhla ERNIE-RNA frozen F1-skóre 0,646 na bpRNA-new a 0,590 na RNA3DB-2D, čímž překonala tradiční metody dynamického programování jako Eternafold (0,639) a udržela si převahu nad všemi konkurenty hlubokého učení. ERNIE-RNA také dosáhla lepšího výkonu v různých downstream úlohách: predikce kontaktní mapy RNA s přesností Top-L/1 0,68 (oproti souboru RNAcontact 0,46), 5'UTR MRL predikce s R² 0,92 na náhodné testovací sadě a 0,86 na lidské testovací sadě, predikce vazby RNA-proteinu překonávající všechny testované metody, přesnosti klasifikace rodiny ncRNA 0,9844 (0% hraniční šum) a 0,9820 (200% hraniční šum), F1 skóre predikce lokality splice v rozmezí od 0,9180 do 0,9612 napříč čtyřmi druhy, top-K přesnost 55,37 % na datové sadě SpliceAI (oproti 34,84 % RNA-FM) a alternativní predikce polyadenylace R² 78,39 % (oproti 70,32 % RNA-FM).
Autoři: Weijie Yin, Zhaoyu Zhang, Shuo Zhang, Liang He a další. al Xuegong Zhang, Tao Qin a Zhen Xie
Propojit:

2,34K
Může umělá inteligence navrhnout terapeutické peptidy napodobením toho, jak se přírodní proteiny vážou na cíle onemocnění?@Tsinghua_Uni @natBME
"Design peptidů prostřednictvím mimikry vazebného rozhraní s PepMimic"
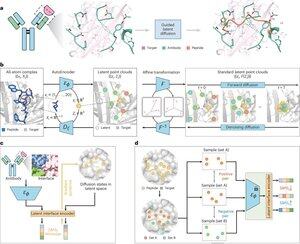
• Výzkumníci vyvinuli PepMimic, algoritmus umělé inteligence, který kombinuje autokodér všech atomů, model latentní difúze a kodér rozhraní pro návrh peptidů (4-25 aminokyselin), které napodobují vazebná rozhraní mezi cílovými proteiny a známými pojivy, jako jsou protilátky nebo receptory, a řeší omezení současného designu peptidů, který vyžaduje manuální znalosti a bojuje s nespojitými vazebnými povrchy.
• Více než 80 peptidových terapeutik je schváleno pro nemoci včetně cukrovky a rakoviny, která nabízejí výhody, jako je vysoká specificita, nižší toxicita a potenciální perorální podání ve srovnání s malými molekulami a biologiky, přesto navrhování peptidových napodobenin protein-proteinových interakcí tradičně vyžaduje rozsáhlé odborné znalosti a nemůže efektivně zvládnout nespojitá vazebná rozhraní, zatímco stávající modely umělé inteligence se zaměřují spíše na přístupy typu páteř a poté než na zachycení klíčového postranního řetězce. geometrie pro přesné interakce aminokyselin.
PepMimic byl vyškolen na 4 157 protein-peptidových komplexech a 70 645 fragmentech podobných peptidům z Proteinové databanky, pomocí autoenkodéru pro mapování geometrií všech atomů do latentního prostoru, difúzního modelu pro 100 kroků odšumování a kontrastivního učení pro trénování kodéru rozhraní, který řídí generaci minimalizací vzdáleností mezi navrženým a referenčním rozhraním v latentním prostoru, přičemž kandidáti jsou seřazeni pomocí energie rozhraní Rosetta. Energie FoldX, metriky zásahu rozhraní a skóre AlphaFold Multimer pLDDT před výběrem nejlepších peptidů (384 pro cíle se známými pojivy, 94-290 pro pojiva generovaná umělou inteligencí) pro experimenty se zobrazováním rezonance povrchových plazmonů.
• PepMimic dosáhl průměrného AUROC 0,71 v 31 úkolech na 93 testovacích komplexech (překonal RFDiffusion 0,69), navrhl 384 peptidů pro 5 cílů léčiv (PD-L1, CD38, BCMA, HER2, CD4) s 8 % dosahujícími KD < 100 nM a 26 peptidy dosahujícími KD na úrovni 10⁻⁹ M (podstatně vyšší než náhodný screening v knihovně), generoval peptidy napodobující pojiva navržená umělou inteligencí pro CD38 a TROP2 se 14% úspěšností (16 % pro CD38, 8 % pro TROP2) a prokázal účinné cílení na nádory in vivo na myších modelech s vybranými peptidy, které vykazovaly 8,85krát větší absorpci u PD-L1-pozitivních nádorů a 16,18krát větší absorpci u TROP2-pozitivních nádorů, dosahující úspěšnosti 20 000-90 000krát vyšší než experimentální screening náhodných knihoven.
Autoři: Xiangzhe Kong et. al Zihua Wang, Yang Liu & @musicsuperman
Propojit:
19,07K
Top
Hodnocení
Oblíbené













