Chủ đề thịnh hành
#
Bonk Eco continues to show strength amid $USELESS rally
#
Pump.fun to raise $1B token sale, traders speculating on airdrop
#
Boop.Fun leading the way with a new launchpad on Solana.

DailyHealthcareAI
Chia sẻ các tài liệu nghiên cứu và tin tức về các ứng dụng AI trong X quang, bệnh học, di truyền học, thiết kế protein và nhiều hơn nữa. Hãy cùng nhau tìm hiểu nhé!
🚀David Baker preprint từ @UWproteindesign 👇👇
Điều gì khiến việc cắt đứt liên kết protein trở nên khó khăn đến mức tự nhiên đã phát triển các enzyme chuyên biệt với các yếu tố đồng kim loại để thực hiện điều đó?@biorxivpreprint @ETH_en
"Thiết kế tính toán của các protease cysteine"
• Các liên kết amide trong protein có thời gian bán hủy hàng trăm năm dưới các điều kiện sinh lý, khiến chúng ổn định hơn nhiều so với các liên kết ester (với các nhóm rời amine có pKa >35 so với <8 cho các ester hoạt hóa), và thiết kế enzyme tính toán trước đây chỉ thành công với các chất nền ester phân tử nhỏ đã được kích hoạt thay vì việc cắt đứt liên kết peptide đòi hỏi năng lượng cho các protease.
• Các nhà nghiên cứu đã sử dụng RoseTTAFold Diffusion 2 cho các Giao diện Phân tử (RFD2-MI) để thiết kế các protease kẽm từ các motif xúc tác tối thiểu, xây dựng một vị trí hoạt động lý tưởng với năm nhóm chức năng (ba dư lượng liên kết kẽm H1, H2, E1, một bazơ xúc tác E2, và một tyrosine Y ổn định oxyanion) dựa trên cấu trúc aminopeptidase N và astacin, thực hiện thiết kế hai chiều cho cả chuỗi protease và chất nền để đảm bảo vị trí chính xác của liên kết amide mục tiêu.
• Trong số 135 thiết kế được thử nghiệm trong một vòng thiết kế duy nhất, 36% cho thấy hoạt động (14.7% cho các mô hình chỉ có Zn và 87.5% cho các mô hình Zn-nước), với tất cả các thiết kế hoạt động đều cắt đứt chính xác tại các vị trí dự kiến được xác nhận bằng khối phổ; thiết kế hoạt động nhất (Zn45 cắt đứt chất nền ZnO36) đạt kcat là 0.025 ± 0.002 s⁻¹, KM là 26 ± 5 μM, và kcat/KM là 900 ± 200 M⁻¹s⁻¹, đại diện cho sự gia tốc tỷ lệ >10⁸ lần so với thủy phân không xúc tác; các thiết kế thể hiện sự liên kết kẽm với Kd giữa 10⁻¹⁰ và 10⁻⁸ M, cho thấy tính đặc hiệu của chất nền trong 4 trên 5 khung, và có thể được lập trình lại để cắt đứt protein TDP-43 của con người liên quan đến bệnh với 4 biến thể đạt ≥80% cắt đứt sau 5 giờ.
Tác giả: Hojae Choi et. al Donald Hilvert, Samuel J. Pellock, David Baker
Liên kết:

615
Mô hình ngôn ngữ có thể học cấu trúc RNA mà không cần dữ liệu huấn luyện cấu trúc rõ ràng không?@NatureComms @Tsinghua_Uni
"ERNIE-RNA: một mô hình ngôn ngữ RNA với các đại diện được tăng cường cấu trúc"
• Các mô hình ngôn ngữ RNA hiện có thường bỏ qua thông tin cấu trúc trong các chuỗi, dẫn đến việc trích xuất đặc điểm không đầy đủ và hiệu suất không tối ưu, mặc dù RNA có tổ chức phân cấp nơi các chuỗi chính gập lại thành các hình dạng cấu trúc cụ thể xác định chức năng sinh học. Các phương pháp tính toán truyền thống cho dự đoán cấu trúc RNA gặp phải những thách thức riêng: các phương pháp dựa trên nhiệt động học bị hạn chế bởi độ chính xác của tham số, các phương pháp dựa trên căn chỉnh gặp khó khăn khi không có đủ chuỗi đồng hình, và các mô hình học sâu cho thấy khả năng tổng quát hạn chế đối với các gia đình RNA chưa thấy. Trong khi các mô hình ngôn ngữ RNA kiểu BERT như RNA-FM (được huấn luyện trên 23 triệu chuỗi), UNI-RNA (1 tỷ chuỗi, 400 triệu tham số), và RiNALMo (36 triệu chuỗi, 650 triệu tham số) đã xuất hiện, chúng không thể tích hợp thông tin cấu trúc một cách đầy đủ, với một số như UTR-LM cố gắng giải quyết điều này bằng cách tích hợp các cấu trúc dự đoán từ RNAfold nhưng gặp phải những hạn chế từ lỗi dự đoán và khả năng tổng quát giảm.
• ERNIE-RNA là một mô hình ngôn ngữ RNA được tiền huấn luyện với 86 triệu tham số dựa trên kiến trúc BERT đã được sửa đổi với 12 khối transformer và 12 đầu chú ý, được huấn luyện trên 20,4 triệu chuỗi RNA không mã hóa từ RNAcentral sau khi lọc các chuỗi dài hơn 1022 nucleotide và áp dụng loại bỏ độ trùng lặp CD-HIT ở mức độ tương đồng 100%. Mô hình này tích hợp một cơ chế thiên lệch chú ý thông tin về cặp cơ sở, gán giá trị 2 cho các cặp AU, 3 cho các cặp CG, và một tham số có thể điều chỉnh α (ban đầu là 0.8) cho các cặp GU trong ma trận vị trí cặp đôi tất cả với tất cả, thay thế thuật ngữ thiên lệch trong lớp transformer đầu tiên. Tiền huấn luyện sử dụng mô hình ngôn ngữ bị che giấu với 15% các token được thay thế ngẫu nhiên, được huấn luyện trong 20 ngày trên 24 GPU 32G-V100 sử dụng fairseq với tốc độ học cơ bản 0.0001, 20.000 bước khởi động, và 0.01 giảm trọng số, tạo ra cả bản đồ chú ý (L×L×156) và nhúng token (12×768×L) như là đầu ra.
• Các bản đồ chú ý của ERNIE-RNA đã chứng minh khả năng dự đoán cấu trúc thứ cấp RNA không cần tinh chỉnh với điểm F1 trung vị là 0.552 trên tập kiểm tra bpRNA-1m, vượt trội hơn RNAfold (0.492), RNAstructure (0.491), RNAErnie (0.440), và RNA-BERT (0.365) mà không cần tinh chỉnh. Sau khi tinh chỉnh, ERNIE-RNA đạt được điểm F1 trung bình macro hiện đại là 0.873 trên bpRNA-1m, vượt qua RiNALMo (0.850, 650 triệu tham số) và UNI-RNA (0.821, 400 triệu tham số), với sự lãnh đạo tương tự trên ArchiveII (0.954 so với 0.892 của RiNALMo) và RIVAS TestSetB (0.721 so với 0.555 của RiNALMo). Trong các bài kiểm tra tổng quát giữa các gia đình khó khăn, ERNIE-RNA đã đạt được điểm F1 là 0.646 trên bpRNA-new và 0.590 trên RNA3DB-2D, vượt trội hơn các phương pháp lập trình động truyền thống như Eternafold (0.639) và duy trì sự vượt trội so với tất cả các đối thủ cạnh tranh học sâu. ERNIE-RNA cũng đạt được hiệu suất vượt trội trên nhiều nhiệm vụ hạ nguồn khác nhau: dự đoán bản đồ tiếp xúc RNA với độ chính xác Top-L/1 là 0.68 (so với 0.46 của RNAcontact), dự đoán MRL 5'UTR với R² là 0.92 trên tập kiểm tra ngẫu nhiên và 0.86 trên tập kiểm tra người, dự đoán liên kết RNA-protein vượt trội hơn tất cả các phương pháp đã thử nghiệm, độ chính xác phân loại gia đình ncRNA là 0.9844 (0% tiếng ồn biên) và 0.9820 (200% tiếng ồn biên), điểm F1 dự đoán vị trí cắt dao động từ 0.9180 đến 0.9612 trên bốn loài, độ chính xác top-K là 55.37% trên tập dữ liệu SpliceAI (so với 34.84% của RNA-FM), và dự đoán polyadenyl hóa thay thế R² là 78.39% (so với 70.32% của RNA-FM).
Tác giả: Weijie Yin, Zhaoyu Zhang, Shuo Zhang, Liang He et. al Xuegong Zhang, Tao Qin & Zhen Xie
Liên kết:

640
Liệu trí tuệ nhân tạo có thể thiết kế các peptide điều trị bằng cách bắt chước cách mà các protein tự nhiên liên kết với các mục tiêu bệnh tật không?@Tsinghua_Uni @natBME
"Thiết kế peptide thông qua việc bắt chước giao diện liên kết với PepMimic"
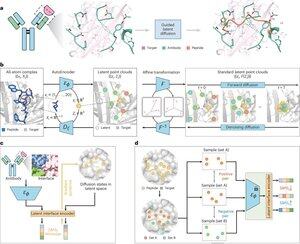
• Các nhà nghiên cứu đã phát triển PepMimic, một thuật toán AI kết hợp giữa autoencoder toàn nguyên tử, mô hình khuếch tán tiềm ẩn và bộ mã hóa giao diện để thiết kế các peptide (4-25 axit amin) bắt chước các giao diện liên kết giữa các protein mục tiêu và các chất liên kết đã biết như kháng thể hoặc thụ thể, giải quyết những hạn chế trong thiết kế peptide hiện tại mà yêu cầu chuyên môn thủ công và gặp khó khăn với các bề mặt liên kết không liên tục.
• Hơn 80 peptide điều trị đã được phê duyệt cho các bệnh như tiểu đường và ung thư, mang lại những lợi thế như độ đặc hiệu cao, độc tính thấp và khả năng sử dụng đường uống so với các phân tử nhỏ và sinh học, tuy nhiên việc thiết kế các peptide bắt chước các tương tác protein-protein truyền thống yêu cầu chuyên môn rộng rãi và không thể xử lý hiệu quả các giao diện liên kết không liên tục, trong khi các mô hình AI hiện có tập trung vào các phương pháp xương sống rồi đến chuỗi thay vì nắm bắt hình học chuỗi bên quan trọng cho các tương tác axit amin chính xác.
• PepMimic đã được đào tạo trên 4,157 phức hợp protein-peptide và 70,645 mảnh peptide-like từ Ngân hàng Dữ liệu Protein, sử dụng một autoencoder để ánh xạ các hình học toàn nguyên tử vào không gian tiềm ẩn, một mô hình khuếch tán cho 100 bước khử nhiễu, và học đối kháng để đào tạo một bộ mã hóa giao diện hướng dẫn việc tạo ra bằng cách giảm thiểu khoảng cách giữa các giao diện thiết kế và tham chiếu trong không gian tiềm ẩn, với các ứng viên được xếp hạng bằng năng lượng giao diện Rosetta, năng lượng FoldX, các chỉ số hit giao diện, và điểm số pLDDT của AlphaFold Multimer trước khi chọn các peptide hàng đầu (384 cho các mục tiêu có chất liên kết đã biết, 94-290 cho các chất liên kết do AI tạo ra) cho các thí nghiệm hình ảnh cộng hưởng plasmon bề mặt.
• PepMimic đạt được AUROC trung bình là 0.71 trên 31 nhiệm vụ trên 93 phức hợp thử nghiệm (vượt trội hơn RFDiffusion với 0.69), thiết kế 384 peptide cho 5 mục tiêu thuốc (PD-L1, CD38, BCMA, HER2, CD4) với 8% đạt KD < 100 nM và 26 peptide đạt KD ở mức 10⁻⁹ M (cao hơn đáng kể so với sàng lọc thư viện ngẫu nhiên), tạo ra các peptide bắt chước các chất liên kết do AI thiết kế cho CD38 và TROP2 với tỷ lệ thành công 14% (16% cho CD38, 8% cho TROP2), và chứng minh hiệu quả trong việc nhắm mục tiêu khối u in vivo trong các mô hình chuột với các peptide được chọn cho thấy sự hấp thụ cao hơn 8.85 lần trong các khối u dương tính với PD-L1 và 16.18 lần trong các khối u dương tính với TROP2, đạt được tỷ lệ thành công cao hơn 20,000-90,000 lần so với sàng lọc thư viện ngẫu nhiên thực nghiệm.
Tác giả: Xiangzhe Kong et. al Zihua Wang, Yang Liu & @musicsuperman
Liên kết:
1,25K
Hàng đầu
Thứ hạng
Yêu thích












